科研动态
51直播
蛋白质稳态维持是细胞生命活动的核心,而蛋白酶体是其主要的“垃圾处理厂”。传统观点认为,蛋白酶体通过识别泛素链标记的底物启动降解。然而,近年来研究发现,部分细胞核蛋白,如即早基因(IEG)产物EGR1、FosB等,存在不依赖泛素的降解通路,其中midnolin作为关键衔接蛋白发挥着核心作用1。然而,midnolin如何将底物精准递送至蛋白酶体,以及蛋白酶体如何识别这一信号并启动降解,仍缺乏深入理解。
2026年3月27日,51直播-51直播网 梁令/林志强团队联合在Nature Communications杂志在线发表题为“Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover”的研究论文。该研究通过冷冻电镜技术解析了midnolin-26S蛋白酶体复合物的多种构象状态,完整揭示了从底物识别、递送到降解的全流程动态机制,阐明了midnolin如何作为一种非经典的降解标签,以不同于泛素的方式将底物蛋白直接递送至蛋白酶体进行降解。这一发现为靶向“难成药”核蛋白的蛋白降解技术研发提供了新思路。

研究团队首先通过HEK293细胞亲和纯化(利用midnolin的标签)发现,midnolin可稳定结合26S蛋白酶体。体外实验进一步表明,midnolin的稳定表达依赖于底物。随后,利用单颗粒冷冻电镜技术,解析了内源纯化及体外孵育条件下midnolin-26S蛋白酶体复合物的多种高分辨率构象状态(图1)。结果显示,midnolin的C端α螺旋(αHelix-C)锚定于蛋白酶体的RPN1亚基,而其泛素样结构域(Ubl)则与蛋白酶体的去泛素化酶RPN11相互作用,这一独特的结合模式将负责底物结合的Catch结构域精准定位于蛋白酶体AAA+马达的入口上方,从而直接引导底物进入降解通道。有趣的是,在缺失Catch结构域的midnolin-蛋白酶体结构中,研究团队发现midnolin自身的N端柔性区域IDR1竟伸入了蛋白酶体的降解通道(图1)。这一意外发现为midnolin的自身降解提供了直接的结构证据,暗示细胞内可能存在一种自我调控机制,以精确控制midnolin的活性水平。
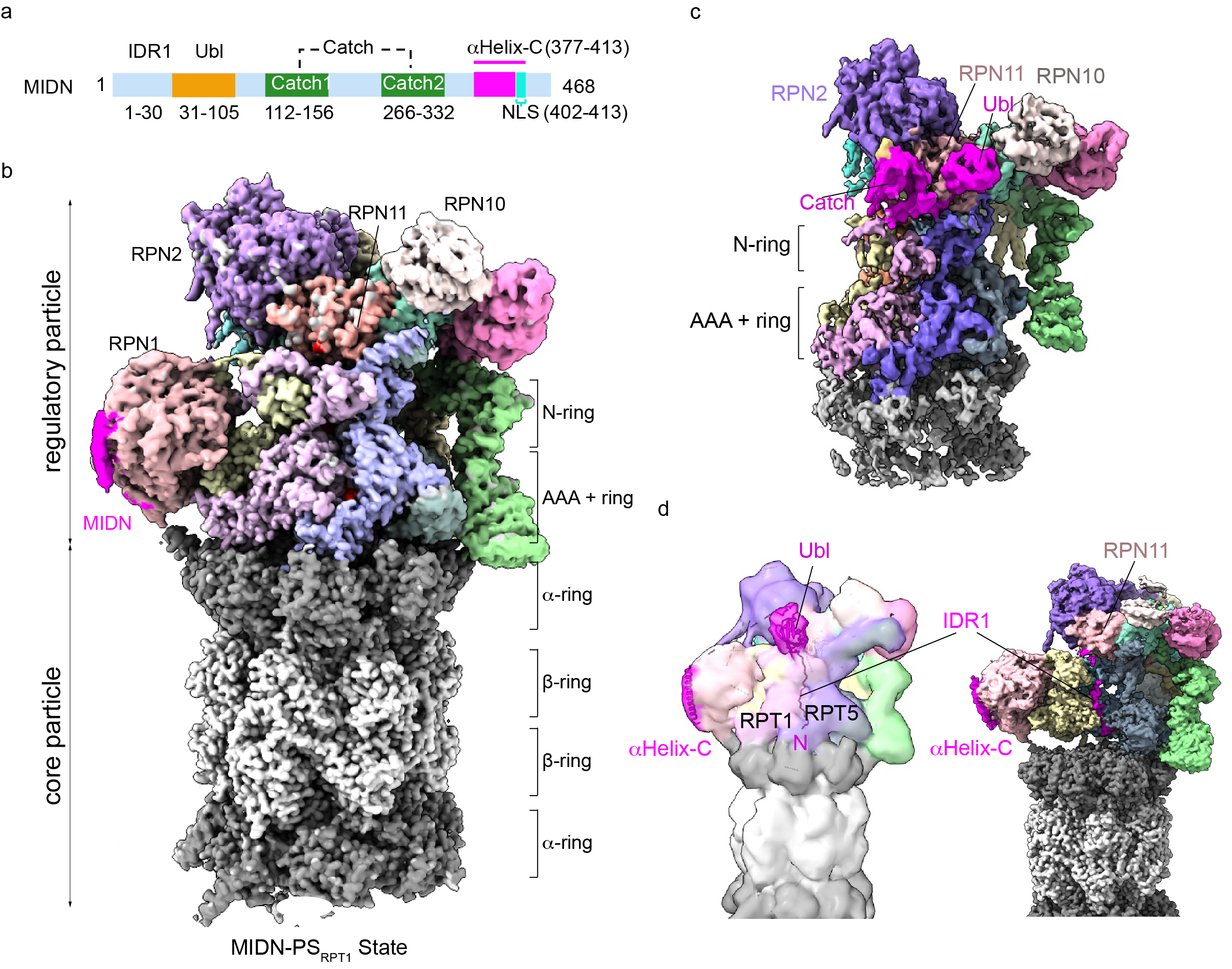
图1Midnolin-蛋白酶体复合物的结构
a. Midnolin(MIDN)结构示意图;b. Midnolin-蛋白酶体底物处理状态整体结构;c. Midnolin-EGR1-蛋白酶体复合物结构;d. Catch结构域缺失midnolin-蛋白酶体结构。
对于内源纯化的全长midnolin-26S蛋白酶体复合物,研究团队通过精细的三维分类,成功捕捉到四种连续的螺旋阶梯构象,如同一部“分子电影”逐帧展示了AAA+ ATP酶六聚体如何一步步将底物向下拉动。尤为重要的是,研究发现镁离子的释放与ATP水解之间存在潜在协同关系,二者共同驱动底物在降解通道中的移位(图2)。
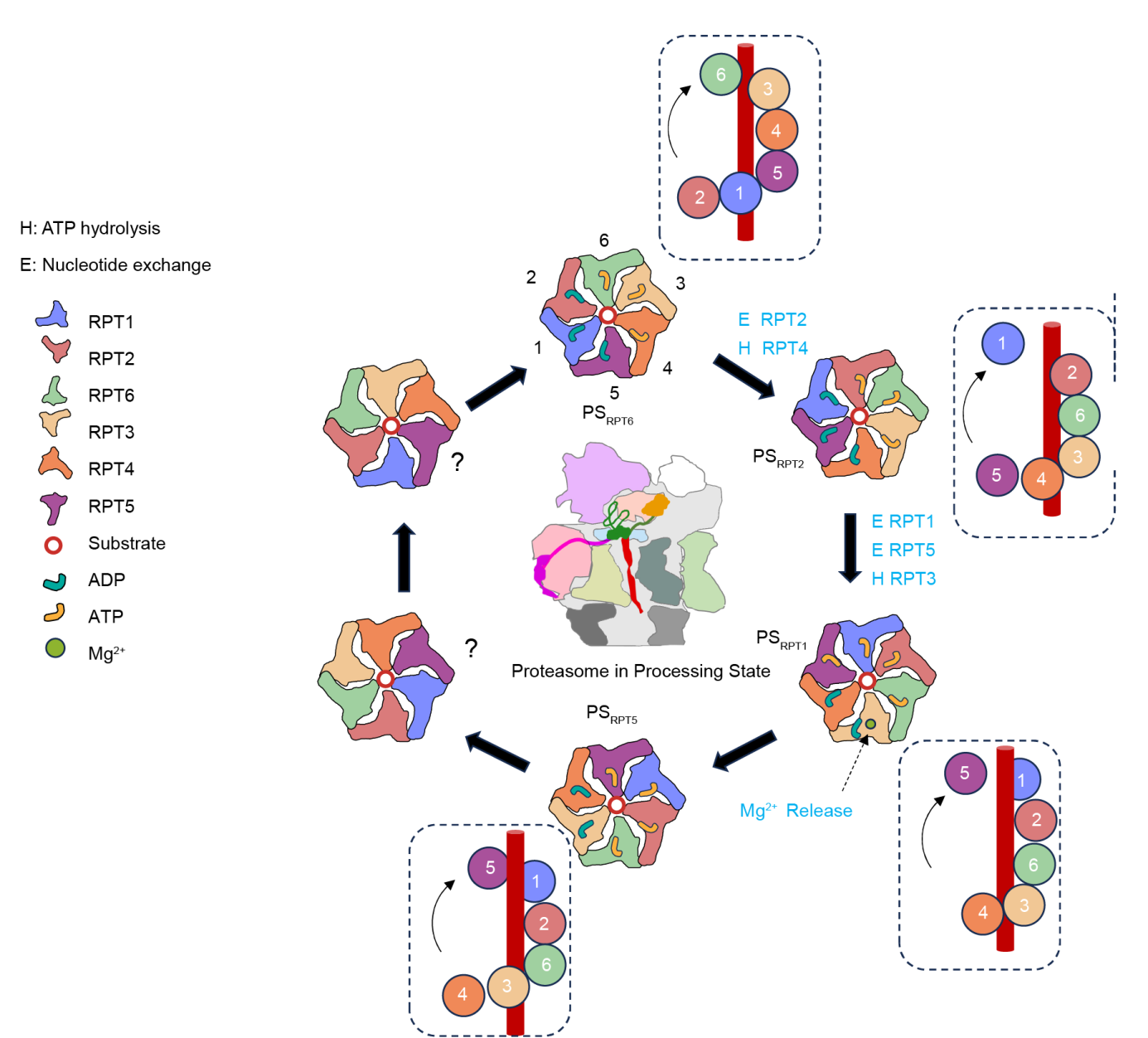
图2Midnolin-蛋白酶体在底物加工过程中的动态构象示意图
值得一提的是,midnolin不仅识别底物,更具备主动“喂食”功能。研究人员巧妙地将Catch结构域替换为底物,发现缺失Catch结构域的突变体虽可结合蛋白酶体,但降解效率显著降低,证实该结构域能确保底物以最佳构象朝向蛋白酶体入口。这一发现为基于midnolin架构的新型靶向蛋白降解剂理性设计提供了理论依据,有望推动难成药靶点的药物开发。
基于以上研究结果,该团队提出midnolin的工作模型(图3):在一定条件下,midnolin与底物共表达并形成稳定复合物;随后,midnolin通过αHelix-C结合蛋白酶体RPN1,Ubl结构域结合RPN11,将Catch结构域及底物精确递送至AAA+马达入口;底物被逐步转运至20S核心颗粒降解后,midnolin自身的无序区域引导其进入蛋白酶体完成自我降解,从而实现核心资源蛋白酶体的循环利用。这一机制既保障了核内蛋白的快速清除,又避免了midnolin的过度累积。
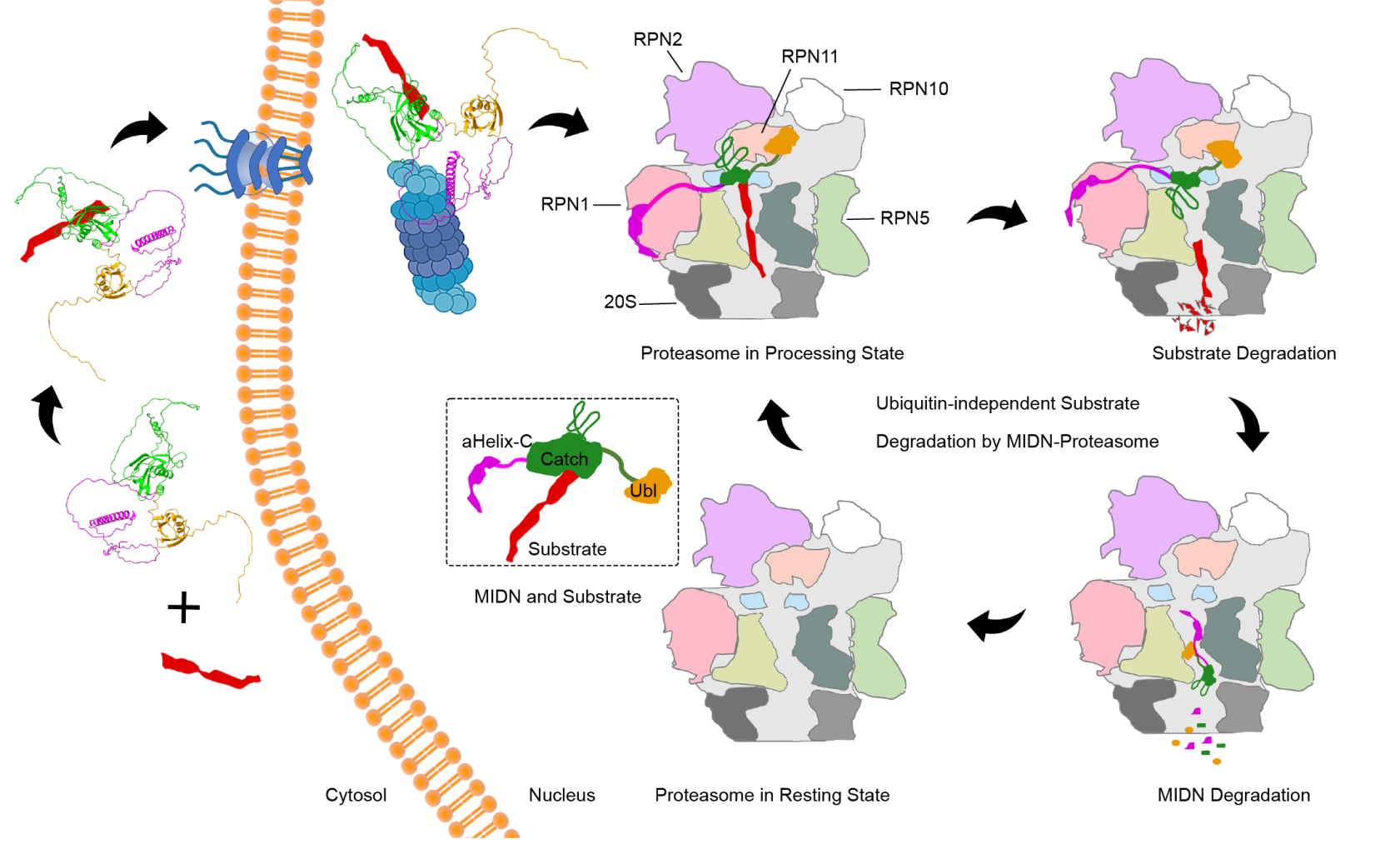
图3 Midnolin工作模型示意图
51直播-51直播网 梁令副研究员和林志强研究员为论文的共同通讯作者。51直播-51直播网 博士研究生祝传达和秦露为论文的共同第一作者。该研究得到了国家自然科学基金、北京市自然科学基金等项目的资助。
原文链接:
//doi.org/10.1038/s41467-026-71002-0
1. Gu, X. et al. The midnolin-proteasome pathway catches proteins for ubiquitination-independent degradation. Science381, eadh5021, doi:10.1126/science.adh5021 (2023).

