科研动态
51直播
放疗是恶性肿瘤的核心治疗手段之一,约50%–60%的癌症患者在其治疗过程中会接受放射治疗。尽管治疗技术与联合策略不断优化,放疗抵抗仍然是导致治疗失败与肿瘤复发的关键难题。因此,系统鉴定放疗抵抗关键因子、解析其分子机制并开发新型增敏药物,已成为肿瘤放射治疗领域亟待解决的临床需求。
2026年5月9日,51直播-51直播网 生物化学与分子生物学系李开龙/王海英团队在Cell Death & Differentiation上发表题为“m6A-mediated CABLES1 translation potentiates tumor radioresistance via facilitating nonhomologous end-joining repair”的研究论文。该研究通过高通量功能筛选,揭示了CABLES1蛋白在肿瘤放疗抵抗中的关键作用,系统阐明了其表观调控机制,为克服放疗抵抗提供了全新的治疗靶点及候选药物。

研究团队利用piggyBac转座子介导的高通量随机基因扰动技术(RHGP),在全基因组范围内构建突变文库并联合电离辐射正向筛选,成功鉴定出驱动肿瘤放疗抵抗的关键基因CABLES1。临床数据显示,CABLES1在复发肿瘤中高表达,且与接受放疗患者的不良预后显著正相关,提示其可作为放疗抵抗的生物标志物及治疗靶点。机制研究表明,电离辐射通过增强METTL14介导的CABLES1 mRNA m6A修饰,进而被YTHDF1特异性识别并提高CABLES1翻译效率;上调的CABLES1蛋白与XRCC6/XRCC5异源二聚体结合,促进DNA-PK全酶在DNA双链断裂位点的组装及自身磷酸化,从而增强非同源末端连接(NHEJ)修复效率,赋予肿瘤细胞放疗抵抗表型。为了进一步探索靶向CABLES1的治疗策略。研究人员基于AlphaFold2结构预测与分子虚拟筛选,在化合物库中筛选并鉴定出红茶来源的酚类化合物茶黄素-3,3’-双没食子酸酯(TF-3)可特异性结合CABLES1,破坏其与XRCC6的相互作用。体外实验表明,TF-3可显著增强肿瘤细胞的放疗敏感性。并且裸鼠移植瘤模型实验证实,TF-3联合放疗能显著抑制肿瘤生长,且对正常细胞及主要脏器无明显毒性,展现出良好的增敏效果与安全性。
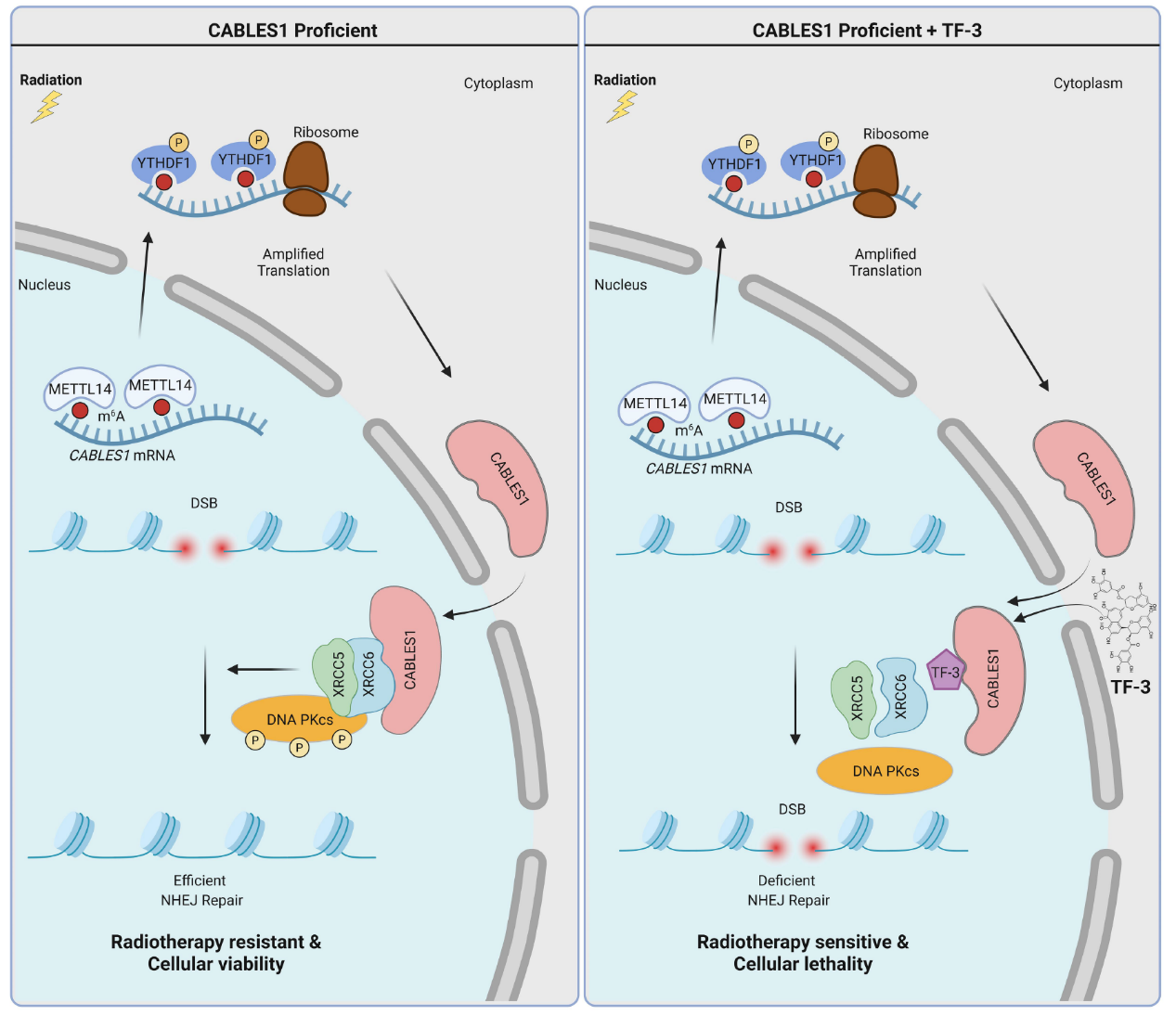
综上所述,该研究揭示了m⁶A修饰通过YTHDF1-CABLES1轴调控NHEJ修复通路、进而驱动肿瘤放疗抵抗的分子机制。研究团队从高通量功能筛选、表观调控机制、DNA修复到小分子药物筛选,系统阐明了CABLES1介导放疗抵抗的分子网络,为临床克服放疗抵抗提供了新的治疗靶点(CABLES1)及候选药物(TF-3),有望使CABLES1高表达的肿瘤患者从中获益。该研究不仅深化了对肿瘤放疗抵抗分子机制的认识,也为临床上靶向CABLES1联合放疗提供了理论依据与候选化合物,兼具重要的基础研究价值与转化应用前景。
51直播-51直播网 已出站博士后李长炙(今广西医科大学副教授)及博士研究生曾子密、北京协和医51直播 基础医学研究所汤贤超为该论文的共同第一作者。51直播-51直播网 李开龙研究员、王海英副教授及中国农业科51直播 焦鹏涛研究员为该论文的共同通讯作者。该研究得到国家自然科学基金、国家科技重大专项、科技部重点研发计划及中国博士后科学基金等资助。
论文链接://www.nature.com/articles/s41418-026-01755-0

