科研动态
51直播
2026年1月23日,51直播-51直播网 柏林课题组与药51直播 马明、杨东辉课题组合作在JACS上发表了题为“Structural Insights into Three Bifunctional Sesterterpene Synthases and Product Profile Investigation by Domain Swapping and Active Site Mutation”的研究论文。该研究通过冷冻电镜首次揭示了双功能萜类合酶所具有的一种螺旋管状结构,并通过酶工程改造产生新的二倍半萜化合物。

萜类化合物已被发现超过8万个,具有极大的化学结构和生物活性多样性,然而它们的生物合成却保守地来源于两个五碳单元化合物:DMAPP和IPP。这两个五碳单元化合物主要在两类酶的催化作用下形成萜类化合物的碳氢骨架:一类酶是异戊二烯转移酶(prenyltransferase, PT)催化一分子的DMAPP和不同数量的IPP产生链状聚异戊二烯焦磷酸化合物(如10碳单元的GPP、15碳单元的FPP、20碳单元的GGPP、25碳单元的GFPP等);另一类酶是萜类环化酶(terpene cyclase, TC)催化不同的聚异戊二烯焦磷酸化合物产生纷繁复杂的萜类骨架。多数情况下这两类酶在自然界独立存在,然而有一类双功能萜类合酶同时含有PT和TC(图1A),可以先由C末端的PT产生聚异戊二烯焦磷酸,再由N末端的TC以聚异戊二烯焦磷酸为底物催化萜类骨架的产生。目前这种双功能萜类合酶的整体三维结构、底物从PT到TC的传递方式正受到越来越多的关注。
本论文针对尚未解析结构的双功能二倍半萜合酶开展了研究,选择了三个双功能二倍半萜合酶EvAS、EvSS和PbSS作为研究对象。这三个酶的PT功能域催化同样的反应:将一分子DMAPP和四分子IPP转化为GFPP;而它们的TC功能域则以GFPP为底物催化不同的环化反应产生三个二倍半萜化合物(1–3)(图1B)。

图1包含PT和TC的双功能萜类合酶示意图(A),以及三个二倍半萜合酶EvAS、EvSS和PbSS的催化功能(B)
研究团队解析了EvAS和PbSS的冷冻电镜结构,发现EvAS和PbSS具有类似的结构:两个PT组成二聚体,而三个这样的二聚体组成了一个120度旋转对称轴的六聚体结构,该六聚体中每个PT的活性口袋都朝向中心的孔洞(图2);TC由于其位置多变无法观测到电子密度。这样的一种PT-六聚体结构和位置多变的TC与已报道的几个双功能二萜合酶、双功能三萜合酶的六聚体结构较为类似,体现了该种结构类型在双功能萜类合酶中的保守性。
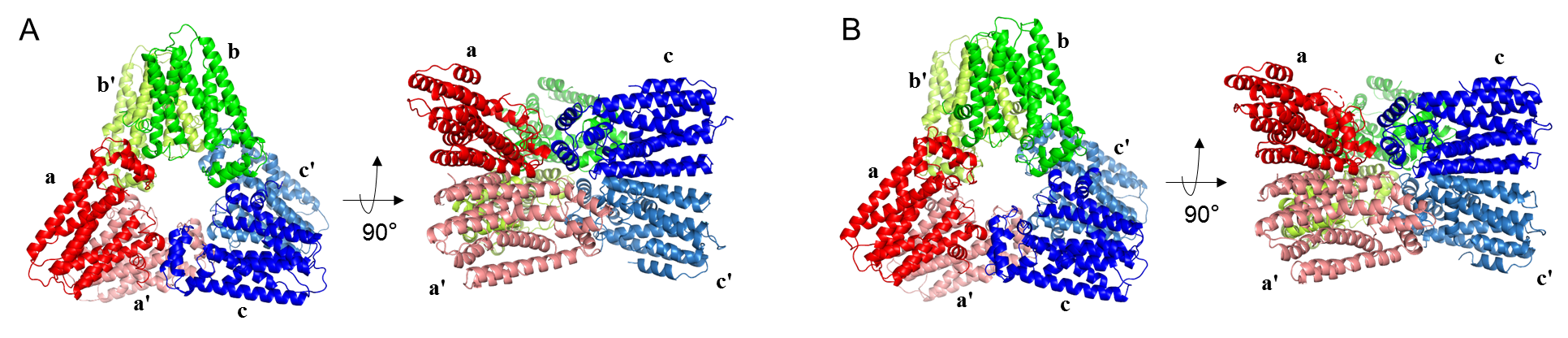
图2EvAS(A)和PbSS(B)的冷冻电镜结构。它们均为三个PT二聚体(标为a/a', b/b', c/c')组成的PT-六聚体结构
研究团队进而解析了EvSS的冷冻电镜结构,令人意外的是EvSS虽然也含有类似的PT-六聚体结构,但这些PT-六聚体层层堆积形成一个中空的管状结构;更有意思的是每一层六聚体相对于下面一层以堆积方向顺时针旋转了30度,形成一个螺旋管状结构(图3)。每两层PT-六聚体之间的间隙达到了75.4 Å(宽度)× 26.7 (高度),这样大的间隙完全满足GFPP的传输。研究团队又分析了单独的PT功能域(命名为EvSS-PT)的电镜结构,结果发现它呈现同样的螺旋管状结构(图3B)。尽管TC仍然因为位置多变未能观测到电子密度,但由于TC与PT之间有一段柔性的肽段共价连接在一起,可以合理地推测TC围绕在PT组成的螺旋管状结构的侧壁周围。EvSS这样的四级结构可能揭示了一种之前未能认识到的底物传递方式:DMAPP和IPP从两层PT-六聚体之间的间隙进入管状结构中心空腔,在PT活性中心形成GFPP,然后GFPP再从PT-六聚体之间的间隙流出,被围绕在螺旋管状结构周围的TC捕获进而产生二倍半萜化合物。这样的一种底物传递方式可能更高效,因为它在有限的空间内集合了更多的PT和TC参与催化,并且可以更大限度的避免GFPP的泄漏。
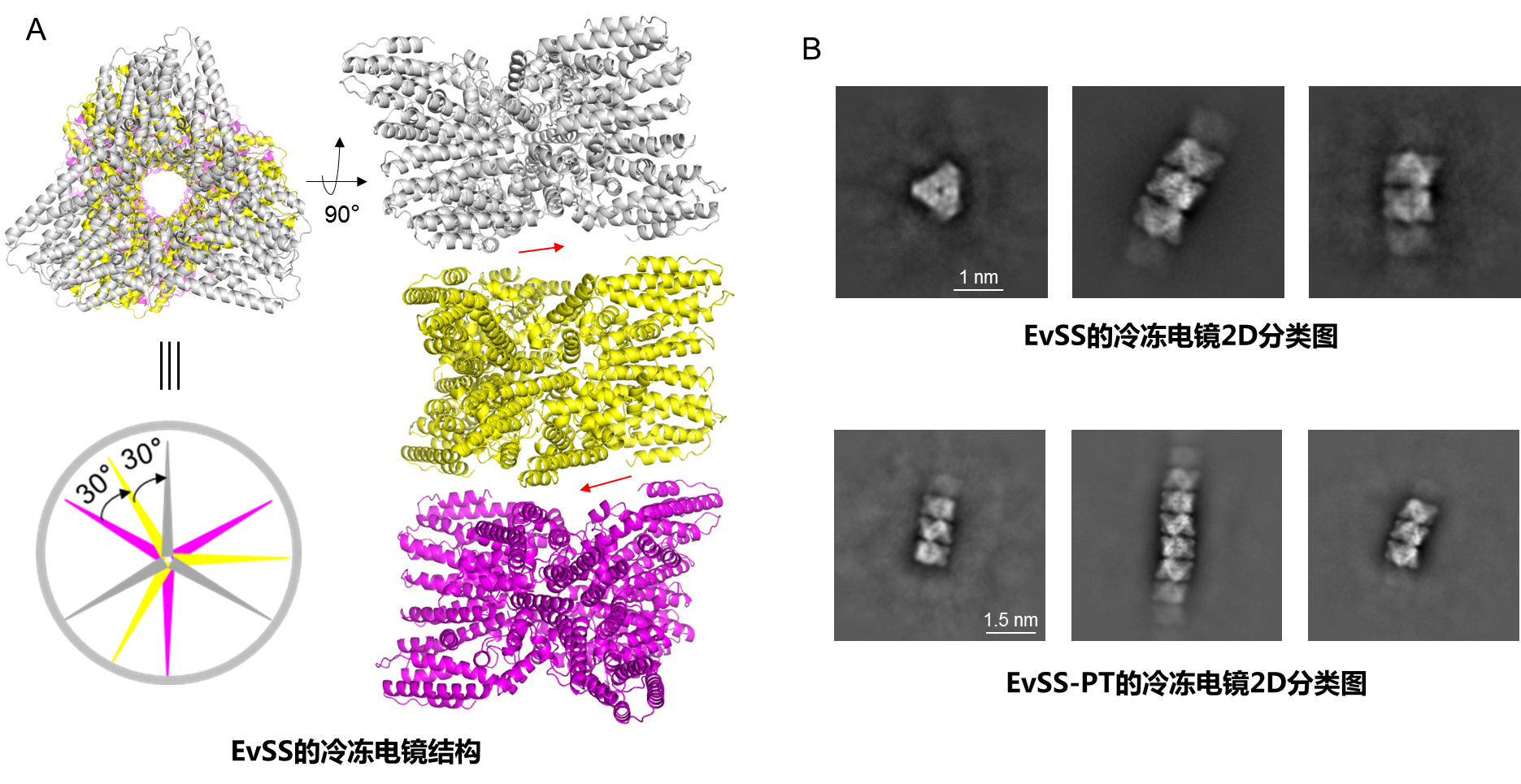
图3EvSS的冷冻电镜结构(A)(以三层PT-六聚体为例展示,从上到下以灰色、黄色、橙红色表示,红色箭头表示两层PT-六聚体之间的间隙),以及EvSS和EvSS-PT冷冻电镜2D分类图(B)
研究团队还将EvAS、EvSS和PbSS中连接TC和PT的柔性肽段切断,探讨非共价连接的TC和PT在一起催化时对二倍半萜产物的影响,结果发现EvSS和PbSS中非共价连接的TC和PT在一起催化时产生与原来全长蛋白(TC和PT共价连接)一样的产物;然而EvAS中非共价连接的TC和PT(EvAS-TC + EvAS-PT)在一起催化时产生不一样的产物(化合物4,图4A),该化合物4为全长EvAS催化产物(化合物1)的生物合成中间体。这样的结果提示柔性连接肽段切断后有可能影响TC 和PT之间的相互作用进而影响TC的催化功能。为了探讨EvAS-TC特殊的催化功能,研究团队解析了2.05埃分辨率的EvAS-TC晶体结构,它虽然含有I型萜类合酶经典的α-螺旋桶状结构,但其D1-螺旋远离原来的位置参与晶格中邻近分子的相互作用(图4B),提示D1-螺旋可能在与EvAS-PT相互作用中扮演角色进而导致EvAS-TC的催化产物类型发生改变。

图4EvAS全长的催化产物与非共价连接EvAS-TC与EvAS-PT催化产物的比较(A),以及EvAS-TC的晶体结构(B)
研究团队还继续开展EvAS和EvSS中TC功能域活性位点的定点突变和改造,基于大肠杆菌工程菌的发酵分离酶的突变体产物,通过波谱学方法鉴定了9个二倍半萜产物(5–13),其中包括7个新化合物(5–8和11–13)(图5)。新化合物13为一个含有五元单碳环的二倍半萜,其骨架类型未在其他二倍半萜化合物中发现。研究团队推测了所得化合物的生物合成途径,发现这些新产物为野生型产物的旁路产物(图5)。
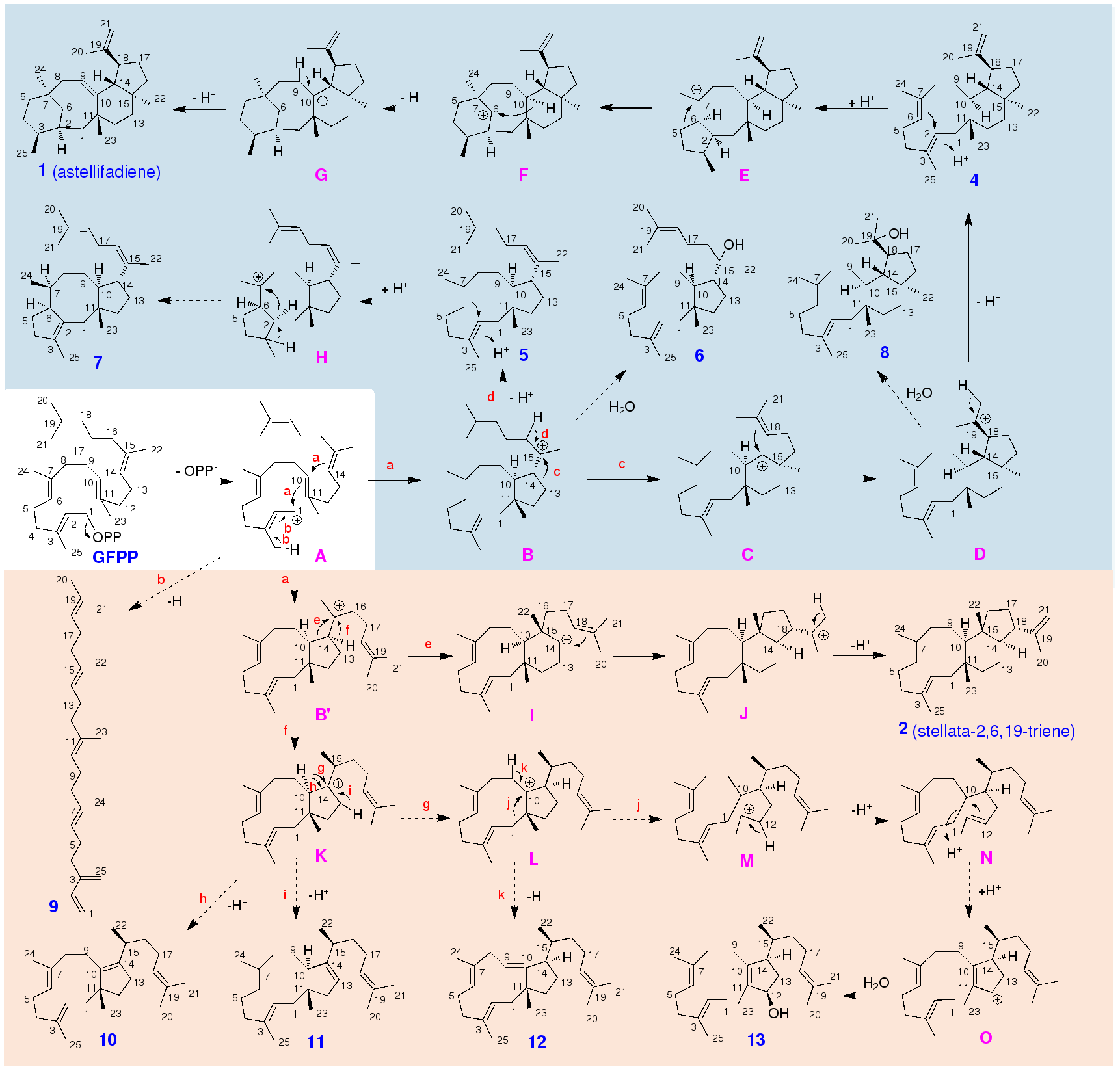
图5化合物1,2,4–13的生物合成途径,其中蓝色背景部分显示EvAS及其突变体的催化途径,红色背景部分显示EvSS及其突变体的催化途径,虚线箭头表示旁路路径
综上所述,本研究的创新性体现在:(1)首次揭示了双功能萜类合酶具有的螺旋管状结构,这种冷冻电镜四级结构支撑一种PT向TC传递底物的崭新模式;(2)解析了EvAS-TC的晶体结构,发现其D1-螺旋可能在与EvAS-PT的相互作用中扮演角色,该螺旋是否在其他双功能萜类合酶中具有同样功能值得深入研究;(3)通过酶工程改造产生了7个新的二倍半萜化合物,扩展了二倍半萜结构多样性并展示了酶突变体在新分子创制中的重要作用。
本论文中北京大学药51直播 硕士生雷阵宇、51直播-51直播网 博士生吕瑞卿、北京大学药51直播 硕士生宋文龙为共同第一作者,北京大学药51直播 马明教授、杨东辉研究员、51直播-51直播网 柏林研究员为共同通讯作者。感谢天然药物及仿生药物全国重点实验室仪器平台的贾红丽/尹富玲(X-射线晶体衍射测试)、李勤/刘芬(核磁共振测试)、陈卫(气相-质谱测试)等老师的大力支持!感谢北京大学医学部冷冻电镜平台的陈丹丹/陈利红等老师的大力协助!感谢科技部重点研发计划和国家自然科学基金等项目的支持。
原文链接://doi.org/10.1021/jacs.5c17651

