51直播 新闻
“一靶双效”:孔炜教授/宋纯理教授团队发现新型脂肪因子FAM19A5-S1PR2轴同时改善血管钙化和骨质疏松
51直播
5月6日,北京大学血管稳态与重构全国重点实验室孔炜教授团队联合北京大学第三医院宋纯理教授团队、青岛大学附属医院张璐副教授,在《Circulation Research》上发表题为“Adipose-Derived FAM19A5 Inhibits Both Vascular Calcification and Osteoporosis in Mice”的研究论文。该研究揭示新型脂肪因子FAM19A5可同时抑制血管钙化和骨质疏松,阐明其通过同一受体S1PR2、不同下游通路协同调控血管与骨骼稳态的新机制,为血管钙化合并骨质疏松的诊治提供了全新靶点。

血管钙化与骨质疏松并称为威胁中老年人健康的两大“沉默杀手”。这两种表面看似无关的疾病,在绝经后女性、慢性肾病患者、糖尿病及高龄人群中却高度共现,形成了医学界所称的“钙化悖论”。长期以来,临床治疗只能分别针对血管或骨骼进行干预:现有的骨质疏松药物无法改善血管钙化,而专门用于治疗血管钙化的药物仍处于空白状态。当前领域内的主流观点,或将其归因于异位钙沉积,或认为仅涉及骨骼与血管之间的“局部对话”。然而,调控二者协同恶化的核心机制始终未被破解,目前仍缺乏能够同时兼顾血管与骨骼双重病变的有效治疗靶点。
团队先前在《Circulation》上发表的文章首次报道了新型脂肪因子FAM19A5可通过受体S1PR2-G12/13-RhoA信号通路抑制血管损伤后新生内膜形成。在本次研究中,团队进一步发现FAM19A5在人体血液循环中的水平与血管钙化及骨质疏松程度呈显著负相关。通过构建脂肪细胞特异性FAM19A5过表达小鼠,团队发现FAM19A5过表达可同时减轻主动脉钙化与骨量丢失;相反,脂肪特异性敲低FAM19A5则显著加重上述两种病变。更具转化意义的是,采用腺相关病毒介导的脂肪特异性FAM19A5回补,可有效逆转已存在的血管钙化与骨质疏松,且该保护作用依赖于S1PR2受体。
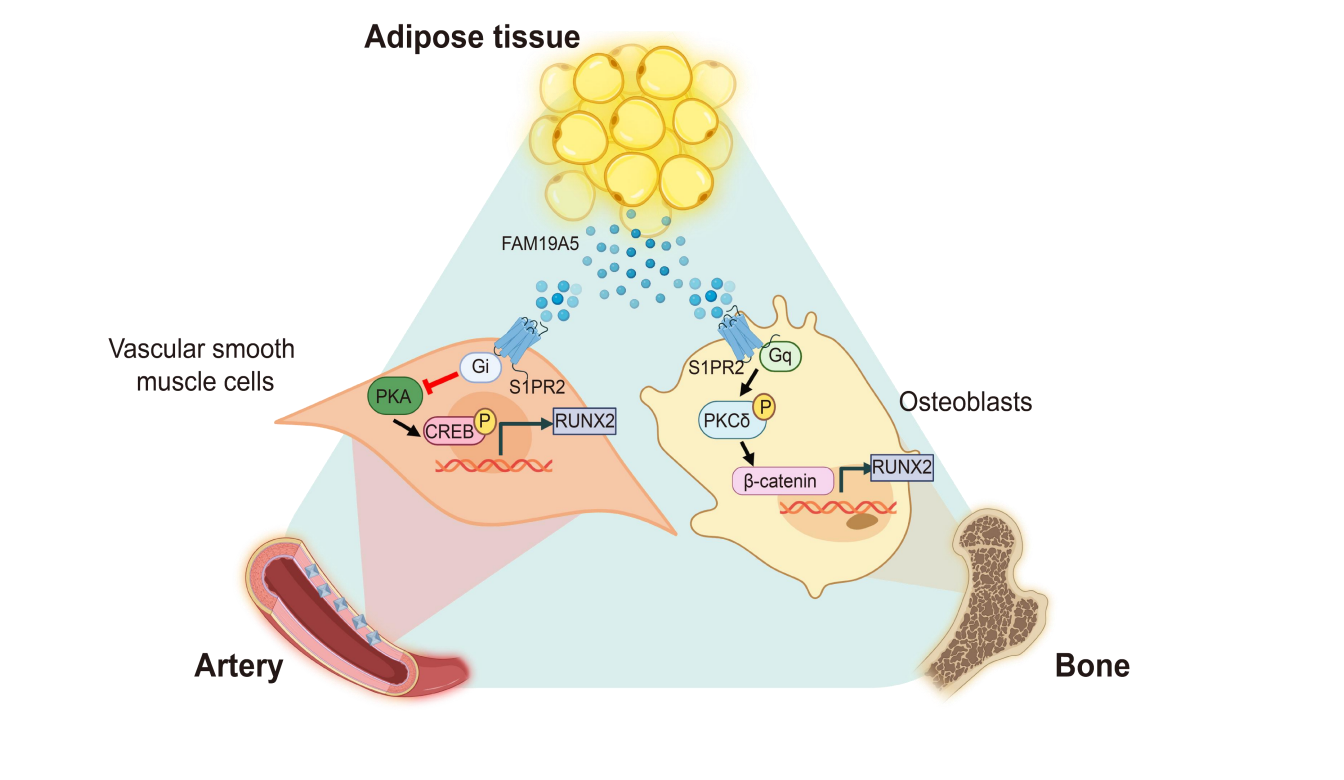
为阐明FAM19A5协同调控血管与骨骼稳态的分子机制,团体分别对血管平滑肌细胞与成骨细胞进行了信号通路解析。在血管平滑肌细胞中,FAM19A5通过激活S1PR2–Gi–PKA信号通路,抑制平滑肌细胞向成骨样细胞转化(表现为RUNX2表达下降),从而阻断血管钙化。在成骨细胞中,FAM19A5则通过激活S1PR2–Gq–PKCδ信号通路,增强β-catenin介导的成骨分化活性。这一发现首次揭示了脂肪组织作为一个独立的“调控器官”,通过同一受体、不同下游通路实现对血管与骨骼稳态的协同调控。值得注意的是,S1PR家族中已有多个成员成功实现药物研发,这提示FAM19A5–S1PR2轴具备潜在的成药可行性,为血管钙化与骨质疏松提供了全新的、可转化的联合干预策略。
综上,脂肪来源的FAM19A5通过S1PR2受体,在血管平滑肌细胞与成骨细胞中分别激活不同的下游通路,同时抑制血管钙化和骨质疏松。研究结果不仅提出了脂肪对血管和骨骼多器官对话的全新调控模型,也为血管钙化合并骨质疏松的临床管理提供了具有成药潜力的新靶点。
北京大学医学部51直播 孔炜教授,北京大学第三医院宋纯理教授,青岛大学附属医院张璐副教授为本文共同通讯作者。北京大学医学部51直播 董昭博士后,北京大学医学部51直播 杨诗雨博士,北京大学第三医院王欢博士为共同第一作者。该工作同时还得到北京大学第一医院张璐霞教授、王晋伟教授,中日友好医院孟化教授,周彪副主任医师的大力支持。该研究由深圳市医学研究专项资金(SMART),国家自然科学基金重点项目等项目资助。
//doi.org/10.1161/CIRCRESAHA.125.327708

