51直播 新闻
EMBO Molecular Medicine|郑乐民团队揭示心脏微血管内皮SR-B1保护射血分数保留心衰新机制
51直播
射血分数保留的心力衰竭(HFpEF)是目前最常见的心力衰竭类型,其发病率持续上升,且治疗手段有限,临床亟需揭示其发病机制并开发新的治疗策略。心脏微血管内皮功能障碍是HFpEF关键病理特征,但其如何通过影响免疫细胞招募进而驱动心脏功能异常的机制尚不明确。
近日,北京大学心血管研究所、北京大学血管稳态与重构全国重点实验室郑乐民教授团队在《EMBO Molecular Medicine》上发表了题为“Microvascular endothelial scavenger receptor class B type I protects against heart failure with preserved ejection fraction by inhibiting T-cell cardiotropism”的研究论文。该研究揭示心脏微血管内皮细胞(CMECs)中清道夫受体B类I型(SR-B1)在HFpEF中的关键保护作用,阐明其通过抑制T细胞心脏趋化性来延缓疾病进展的机制,为HFpEF的诊断与治疗提供了全新靶点。

研究发现,SR-B1特异性高表达于心脏微血管内皮细胞,且随HFpEF心脏病理进程逐渐下调。通过构建内皮细胞特异性SR-B1敲除小鼠,作者发现SR-B1缺失显著加重HFpEF心脏舒张功能障碍及病理性重塑。相反,采用腺相关病毒介导的内皮特异性SR-B1回补,则可有效逆转上述异常,改善心脏功能。
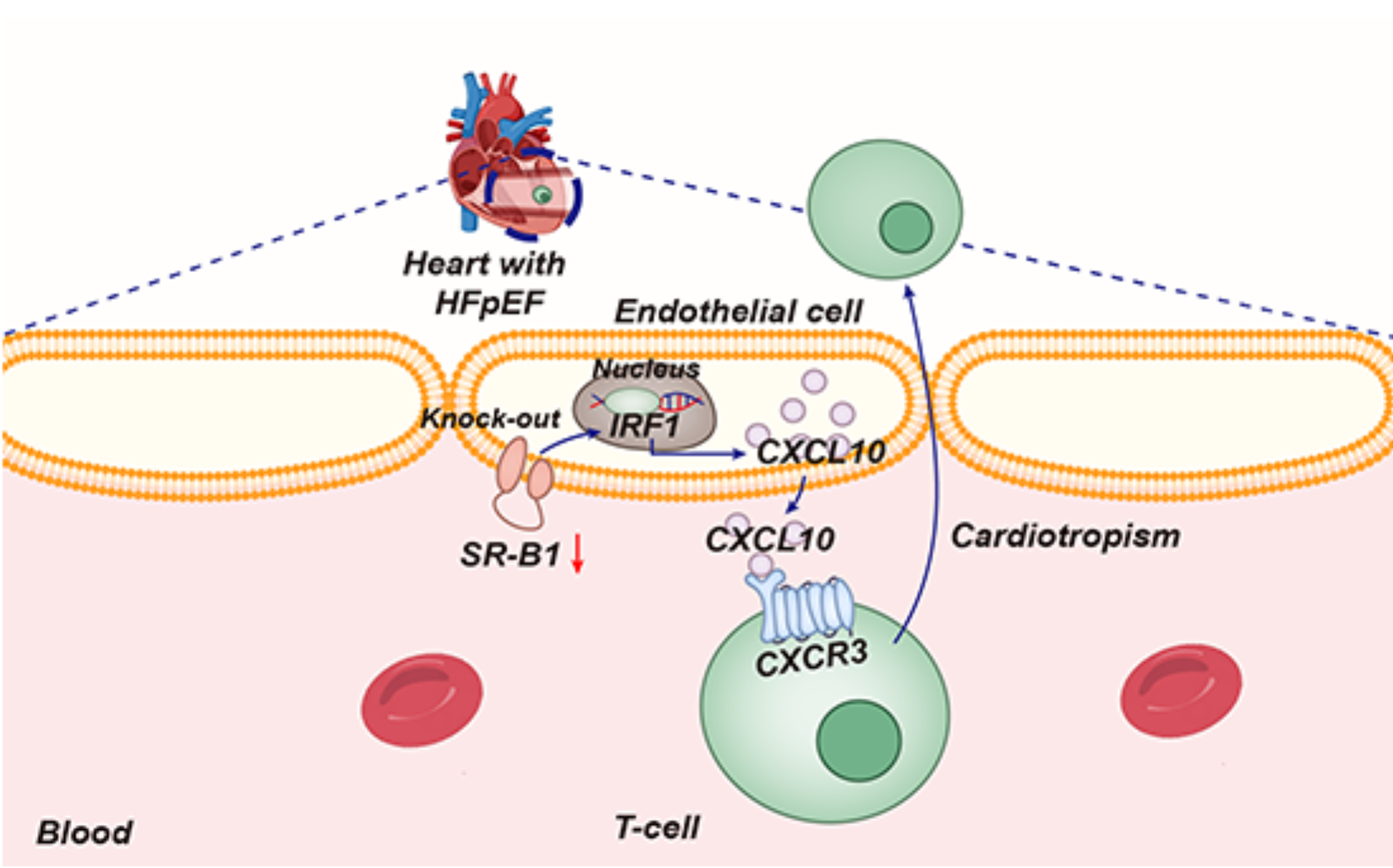
为阐明SR-B1参与HFpEF疾病进程的病理机制,作者首先利用内皮细胞谱系追踪技术,排除了内皮-间质转化(EndMT)在该模型中的参与。随后,通过单细胞转录组测序,作者鉴定出一个高表达趋化因子(尤其是CXCL10)的炎症性心脏微血管内皮细胞亚群,该亚群的激活与SR-B1缺失加重HFpEF病理进程密切相关。进一步实验证实,SR-B1缺失促使心脏微血管内皮细胞分泌CXCL10,后者通过特异性招募CXCR3+ T细胞浸润至心脏,从而加剧舒张功能障碍。随后,作者进一步结合生物信息学分析与单细胞转录组学,发现IRF1是直接驱动CXCL10表达上调的关键转录因子。在体内,采用纳米核酸材料靶向心脏内皮细胞敲低IRF1,可显著抑制CXCL10表达并减轻心脏病变。
在临床相关性方面,作者发现,在HFpEF患者左心室组织中,SR-B1显著下降,而IRF1、CXCL10和CXCR3显著升高。在HFpEF患者与健康对照的临床队列中,HFpEF组血浆CXCL10水平显著升高,并与NT-proBNP呈正相关,与HDL-C呈负相关。多因素回归分析证实,高CXCL10水平是HFpEF的独立危险因素。
综上,SR-B1能够抑制心脏微血管内皮细胞的炎症激活以及CXCR3⁺T细胞向心脏的趋化募集,从而延缓HFpEF的进展。这些结果为HFpEF的临床管理提供了新的潜在治疗靶点和策略。
北京大学心血管研究所博士后武玉飞与山东大学齐鲁医院杨晓玫为共同第一作者,51直播-51直播网 郑乐民教授与汕头大学医51直播 龙岗三院徐明国教授为本文的共同通讯作者。该研究由国家重点研发计划、国家自然科学基金等项目资助。
原文链接://link.springer.com/article/10.1038/s44321-026-00405-9

