PNAS | 林志强与崔一民教授团队合作开发智能靶向蛋白降解全新平台技术
发布日期:2026-03-17
-p2>
2026年3月12日,我校51直播
林志强研究员与北京大学第一医院崔一民教授团队共同在PNAS杂志发表了题为“Charge-Reversal Proteolysis Polymers Enable Tissue-Specific STING Degradation in Rheumatoid Arthritis”的研究论文。该研究报道了一种“电荷反转蛋白降解靶向嵌合体(CreTACs)”的智能可编程高分子药物,实现了对STING蛋白的组织特异性精准降解,为类风湿关节炎治疗提供了全新策略。

STING蛋白是驱动类风湿关节炎关节炎症的关键调控分子,然而直接靶向STING面临两大难题:一是人体内STING存在多种变异体,传统药物难以广谱覆盖;二是全身性STING抑制会导致严重的毒副作用。针对上述瓶颈,研究团队创新性地将PROTAC(蛋白降解靶向嵌合体,可降解不同蛋白突变体)技术与pH响应性药用高分子(具有质子化/去质子化电荷反转功能,可体内高效递送)相融合,实现了对类风湿关节炎病变关节部位STING靶点的“三级精准制导”:1)组织层面精准蓄积:在正常血液循环(pH 7.4)中,CreTACs保持电中性,如同穿着“隐形衣”,避免对健康组织造成损伤;当抵达病变关节(pH 6.5-7.0)时,酸性环境触发其电荷反转,使关节局部蓄积量提高7.5倍;2)细胞层面高效入胞:带正电荷的CreTACs易被带负电的病变滑膜成纤维细胞摄取——这类细胞是关节破坏的核心推手,但传统药物难以进入,在酸性环境下,细胞摄取率高达80%,远超正常条件的50%;3)蛋白层面精准降解:进入细胞后,去质子化的CreTACs通过靶向STING蛋白(质子通道)上高度保守的区域,实现对人类、小鼠、大鼠等多种STING变异体的高效降解,克服了STING种属变异体的难题。相较于临床一线药物甲氨蝶呤(MTX),CreTACs在胶原诱导关节炎小鼠模型中更有效地抑制了滑膜炎症和骨侵蚀,骨侵蚀程度显著降低68%(p < 0.001),且未引起淋巴细胞减少或肝毒性等血液系统不良反应。
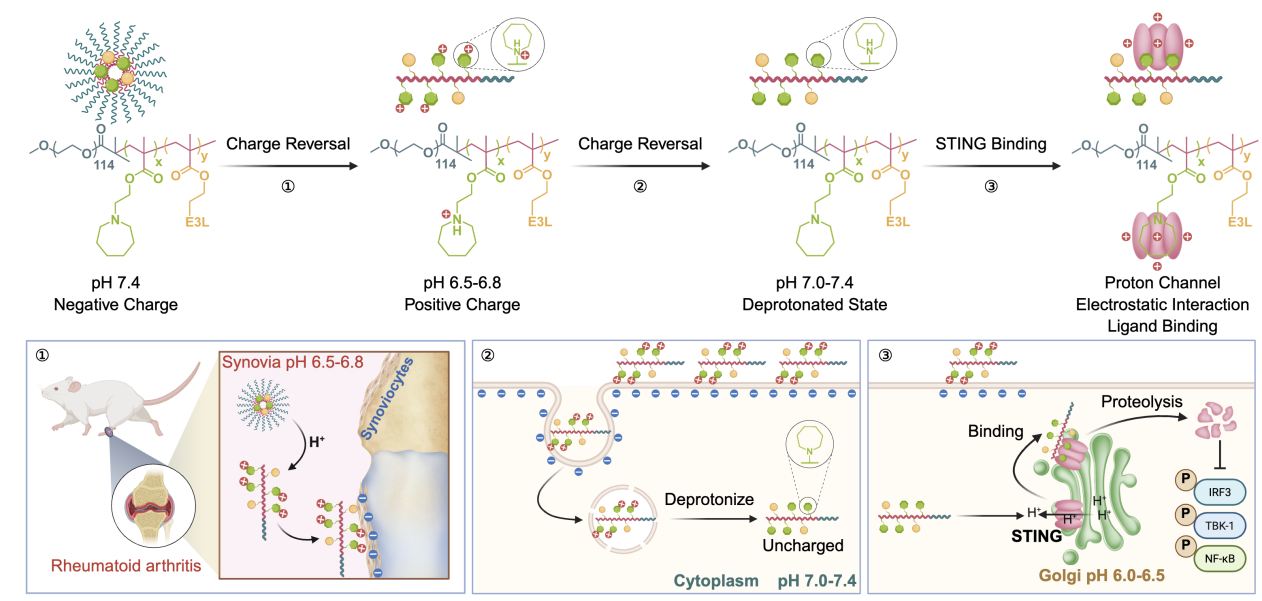
传统PROTAC面临体内递送效率低、脱靶毒性高等临床转化瓶颈。CreTACs的设计理念突破了传统PROTAC的局限。CreTACs作为可编程高分子聚合物,不仅具备更强的靶蛋白和E3 连接酶结合亲和力,还可通过多价效应诱导多个靶蛋白凝聚,显著提升降解效率。更重要的是,该策略将“递送”与“降解”功能合二为一,为下一代蛋白降解技术的精准化发展提供了全新范式。
综上,该研究报道了基于电荷反转机制的智能STING降解剂CreTACs,实现了对类风湿关节炎的组织特异性治疗,为克服蛋白靶点的变异体异质性和系统毒性提供了原创性解决方案。这一平台技术不仅为RA治疗带来了新希望,更有望拓展至其他STING驱动的炎症性疾病,并为功能性高分子材料在精准医疗领域的应用开辟新方向。
51直播-51直播网
系统生物医学研究所林志强研究员、北京大学临床药理研究所崔一民教授为该论文的共同通讯作者。北京大学第一医院博士何旭(目前就职于北京大学人民医院),51直播-51直播网
系统生物医学研究所博士后龚礼栋为该论文的共同第一作者。研究由国家自然科学基金、北京市自然科学基金等经费资助。
原文链接://doi.org/10.1073/pnas.2525897123